Verplaatsingsreactie

- 2194
- 483
- James Dach
We leggen uit wat de verplaatsingsreacties zijn, de typen die bestaan en geven verschillende voorbeelden
 De reactie tussen metalen koper en een zilvernitraatoplossing is een verplaatsingsreactie die kopernitraat (II) produceert (die de oplossing een groenachtig blauwe kleuring geeft) en metalen zilver dat groeit in de vorm van een kleur pluiszilvergrijs
De reactie tussen metalen koper en een zilvernitraatoplossing is een verplaatsingsreactie die kopernitraat (II) produceert (die de oplossing een groenachtig blauwe kleuring geeft) en metalen zilver dat groeit in de vorm van een kleur pluiszilvergrijs Wat is een verplaatsingsreactie?
De Verplaatsingsreactie o Vervangingsreactie is een type chemische reactie waarbij een atoom of een kleine groep atomen in een molecuul wordt vervangen of verplaatst door een ander atoom of groep atomen.
Verplaatsingsreacties kunnen eenvoudig of dubbel zijn en zijn zeer gebruikelijk van aard. Veel van de chemische reacties die we dagelijks zien, zijn verplaatsingsreacties, zoals de sulfatie van terminals in autobatterijen.
Soorten verplaatsingsreacties
Er zijn twee soorten verplaatsingsreacties, eenvoudig en dubbel, die hieronder worden beschreven, samen met enkele specifieke voorbeelden:
Eenvoudige verplaatsingsreactie
Dit zijn verplaatsingsreacties waarbij het ene element een ander vervangt in een chemische verbinding. Ze worden erkend omdat zowel in de reagentia als in de producten er slechts twee stoffen bij betrokken zijn, en in elk geval is een van hen een puur element, terwijl de andere een compound is.
Deze reacties kunnen een van de volgende algemene vergelijkingen hebben:
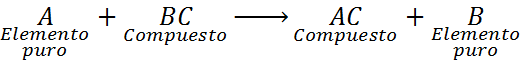
Zoals te zien is, reageert het element A in deze reactie met de BC -verbinding en vervalt of vervangt het element B om de AC -verbinding te vormen.
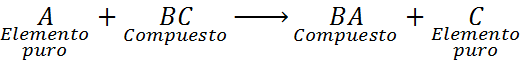
In dit geval reageert element A ook met de BC -verbinding, maar verplaatst of vervangt element C om de BA -verbinding te vormen, waardoor C wordt vrijgeeft in de vorm van een puur element.
Een van de belangrijkste kenmerken om een eenvoudige verplaatsingsreactie te herkennen, is dat het inkomende element uiteindelijk dezelfde plaats moet innemen die het uitgaande element bezet (B of C, zoals het geval is) en dit moet eindigen als een puur element.
Het kan u van dienst zijn: Gallium arseniuro: structuur, eigenschappen, gebruik, risicoOpgemerkt moet worden dat in veel gevallen deel C van het molecuul niet noodzakelijk een individueel element is, maar dat het een groep atomen kan zijn zoals nitraationen (nee3-of sulfaat (dus4-)).
Voorbeelden van eenvoudige verplaatsingsreacties
- Zilveren verplaatsing door koper
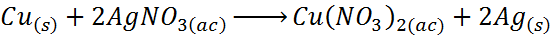
In dit geval werkt koper (Cu) voor element A, zilver (Ag) komt overeen met element B en nitraationen (nee3-) vertegenwoordigen c.
Zoals u kunt zien, vervangt koper in deze reactie zilver in zilvernitraat, waardoor het zilver op een elementaire manier wordt vrijgelaten.
- Sulfatie van batterijterminals

Deze eenvoudige verplaatsingsreactie is wat er gebeurt in terminals of elektrische contacten van veel loodaccumulatoren, dat wil zeggen de batterijen die aanwezig zijn in de meeste benzineauto's.
De reactie wordt bewezen door de vorming van een witte vaste stof die de loodcontacten van deze batterijen bedekt. Zoals te zien is in de vergelijking, is dit een reactie waarbij het lood waterstof in zwavelzuur verplaatst.
- Broomverplaatsing door fluor

In dit geval vervangt fluoride, dat een zeer reactief element is, broom in natriumbromide (NABR) om natriumfluoride (NAF) te vormen. Merk op dat hier het element dat wordt vervangen niet is dat eerst in de samengestelde formule verschijnt, maar dat het de tweede is, zoals in de tweede vorm van de eerder getoonde algemene reactie.
Het kan u van dienst zijn: fractionele destillatie: proces, apparatuur, toepassingen, voorbeeldenDubbele verplaatsingsreactie
Dubbele verplaatsingsreacties, ook wel dubbele vervanging of dubbele ontledingsreacties genoemd, kunnen worden gezien als een uitwisseling van paren. Dit zijn reacties waarbij twee verschillende chemische verbindingen elementen uitwisselen om twee verschillende nieuwe verbindingen te vormen. Deze reacties hebben de volgende algemene vergelijking:
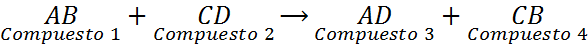
Zoals te zien is in deze algemene reactie, vervangt element A van verbinding 1 (AB) verbinding 2 -element (CD) om verbinding 3 (AD) te vormen. Tegelijkertijd vervangt element C van verbinding 2 (Cd) element A van verbinding 1 (AB) om verbinding 4 (CB) te vormen.
In dubbele verplaatsingen is het essentieel dat de elementen die door elkaar worden vervangen, equivalente posities in de nieuwe verbindingen bezetten. Dit betekent dat, in de algemene reactie, A, die links is en daarom waarschijnlijk een kation is, C alleen C in de CD -verbinding kan vervangen, maar D niet kan vervangen.
Dit is vergelijkbaar met een uitwisseling van dansparen. Als alle paren worden gevormd door een man en een vrouw, moeten de nieuwe paren die na de reactie worden gevormd ook worden gevormd door een man en een vrouw.
Voorbeelden van dubbele verplaatsingsreacties
- Reactie tussen natriumchloride en zilvernitraat

Dit is een duidelijk voorbeeld van een dubbele verplaatsingsreactie. Hier vervangt natrium zilver in zilvernitraat om natriumnitraat te vormen (nano3), Tegelijkertijd dat zilver natrium in natriumchloride vervangt om zilverchloride (AGCL) te vormen.
Het kan je van dienst zijn: Epid- Reactie tussen calciumsulfaat en natriumchloride

In deze dubbele verplaatsingsreactie vervangt calcium natrium in natriumchloride om calciumchloride te vormen, terwijl natrium calcium in calciumsulfaat vervangt om dus natriumsulfaat te vormen.
Een andere manier om deze reactie te zien die even geldig is, is dat sulfaat chloride in natriumchloride vervangt om natriumsulfaat te vormen, terwijl chloride sulfaat vervangt.
Hoewel beide vormen even acceptabel zijn, komt de eerste vaker voor dan de tweede.
- Reactie tussen zwavelzuur en kaliumhydroxide
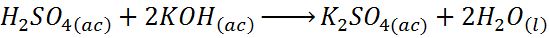
De reactie tussen zwavelzuur en kaliumhydroxide is een op basiszuur gebaseerde neutralisatiereactie, maar het is ook een dubbele verplaatsingsreactie.
In dit geval vervangt waterstof kalium in kaliumhydroxide om water te vormen, terwijl kalium waterstof in zwavelzuur vervangt om kaliumsulfaat te vormen.

