Methoden voor scheiding van homogene mengsels
- 3955
- 991
- Lonnie Rohan
De Methoden voor scheiding van homogene mengsels Het zijn al diegenen die, zonder chemische reacties te gebruiken, het verkrijgen van de componenten of opgeloste stoffen die dezelfde fase integreren toestaan; dat wil zeggen van een vloeistof, vast of gas.
Dergelijke homogene mengsels bestaan uit oplossingen, waarbij opgeloste deeltjes te klein zijn om ze te kunnen onderscheiden met het blote oog. Ze zijn zo klein, dat er geen smalle of selectieve filters zijn om ze te behouden terwijl de oplossing ze overbrengt. Evenmin helpen technieken zoals centrifugatie of magnetisatie uw scheiding.
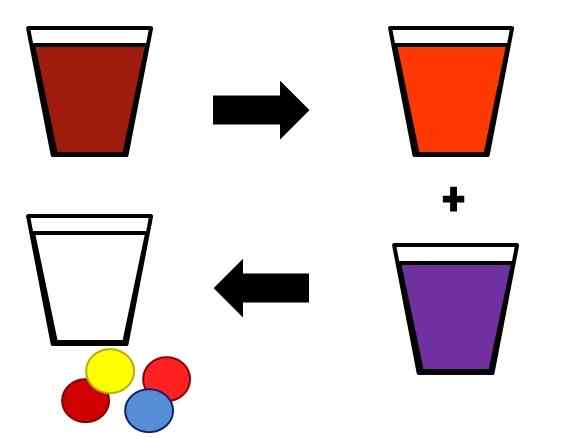 Illustratief voorbeeld van hoe homogene mengsels in fasen kunnen scheiden. Bron: Gabriel Bolívar.
Illustratief voorbeeld van hoe homogene mengsels in fasen kunnen scheiden. Bron: Gabriel Bolívar. Een voorbeeld van hoe oplossingen worden gescheiden in hun componenten wordt hierboven weergegeven. Het initiële mengsel (bruin) is gescheiden in twee componenten, even homogeen (oranje en paars). Ten slotte worden van de twee resulterende mengsels het oplosmiddel (wit) en de vier respectieve paren opgeloste stoffen (roodgeel en roodblauw) verkregen.
Onder de methoden of technieken voor scheiding van oplossingen hebben we verdamping, destillatie, chromatografie en fractionele kristallisatie. Afhankelijk van de complexiteit van het mengsel moet meer dan een van deze methoden worden gebruikt totdat het homogeniteit verbreekt.
[TOC]
De belangrijkste methoden voor scheiding van mengsels
- Verdamping
 Verdamping is de eenvoudigste methode om homogene mengsels te scheiden van een enkele opgeloste stof.
Verdamping is de eenvoudigste methode om homogene mengsels te scheiden van een enkele opgeloste stof. De eenvoudigste homogene mengsels zijn de oplossingen waarbij een enkele opgeloste stof is opgelost. In het superieure beeld is er bijvoorbeeld een kleurrijke oplossing vanwege de absorptie en reflectie van zichtbaar licht met de deeltjes van de opgeloste stof.
Als het tijdens de voorbereiding goed is geroerd, zullen er geen duidelijkere of donkere regio's zijn dan andere; Ze zijn allemaal hetzelfde, uniformen. Dergelijke kleurrijke deeltjes kunnen niet worden gescheiden van het oplosmiddel volgens een mechanische methode, dus u hebt energie nodig in warmte (rode driehoek) om dit te bereiken.
Het kan u van dienst zijn: koolstofdisulfide (CS2): structuur, eigenschappen, gebruik, risico'sAldus wordt de kleurrijke oplossing in de open lucht verwarmd om te versnellen en de verdamping van het oplosmiddel buiten de container mogelijk te maken. Naarmate dit gebeurt, neemt het volume dat de opgeloste deeltjes scheidt af en daarom nemen de interacties toe en eindigen ze langzaam sedimenteren.
Het eindresultaat is dat de kleurrijke opgeloste stof onderaan de container blijft en dat het oplosmiddel volledig is verdampt.
Het ongemak met verdamping is dat, in plaats van opgeloste stoffen, het doel is om het oplosmiddel te elimineren door het op zijn kookpunt te verwarmen. De resterende vaste stof kan uit meer dan één opgeloste stof worden samengesteld en is daarom vereist uit andere scheidingsmethoden om deze te definiëren in zijn geïsoleerde componenten.
- Distillatie
 Distillatie
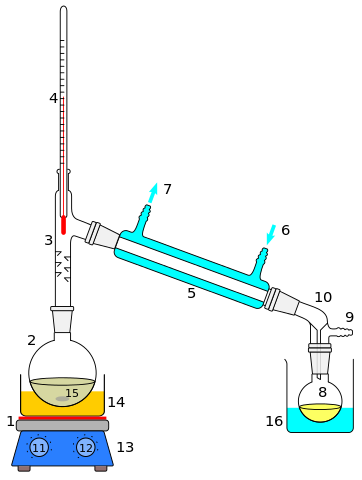
Distillatie Distillatie is misschien de methode voor scheiding van homogene oplossingen of mengsels. Het gebruik ervan strekt zich uit tot gesmolten zouten of metalen, gecondenseerde gassen, oplosmiddelenmengsels of organische extracten. De opgeloste stof is meestal een vloeistof, wiens kookpunt in verschillende graden verschilt ten opzichte van het oplosmiddel.
Wanneer het verschil tussen dergelijke kookpunten hoog is (groter dan 70 ºC), wordt eenvoudige destillatie gebruikt; En zo niet, dan wordt een fractionele destillatie uitgevoerd. Beide destillaties hebben meerdere assemblages of ontwerpen, evenals een andere methode voor mengsels van verschillende chemische aard (vluchtig, reactief, polair, apolar, enz.)).
In destillatie worden zowel oplosmiddel als opgeloste opgeloste stof bewaard, en dit is een van de belangrijkste verschillen met betrekking tot verdamping.
De rotaafaporatie combineert echter deze twee aspecten: een vloeistof-vaste of vloeistof-vloeistofmengsel, zoals dat van een opgeloste en mengbare olie, ze verwarmen tot het oplosmiddel is verwijderd, maar het wordt verzameld in een andere container terwijl de vaste stof of de vaste Olie blijft in de eerste container.
Kan u van dienst zijn: periodiek systeem, waar is het voorLuchtstillatie
Condensaatlucht wordt onderworpen aan cryogene fractionele destillatie om zuurstof, stikstof, argon, neon, etc. te scheiden. De lucht, een homogeen gasachtig mengsel, wordt getransformeerd in een vloeistof waar stikstof, omdat het de meerderheidscomponent is, in theorie als oplosmiddel fungeert; En de andere gassen, ook gecondenseerd, als vloeistof opgeloste stoffen.
- Chromatografie
Chromatografie kan, in tegenstelling tot andere technieken, geen opbrengsten opleveren of op afstand vergelijkbaar zijn; dat wil zeggen, het is niet nuttig om een heel mengsel te verwerken, maar een onbeduidende fractie van hetzelfde. De informatie die het biedt is echter analytisch waardevol, omdat het mengsels identificeert en classificeert op basis van de samenstelling.
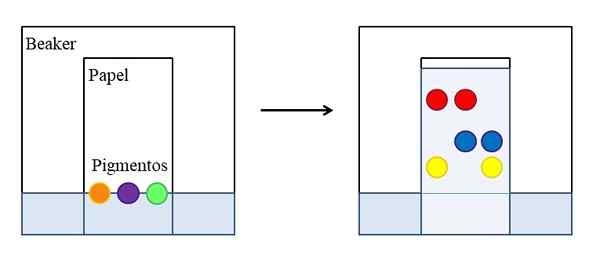 Papier- of fijne laagchromatografie. Bron: Gabriel Bolívar.
Papier- of fijne laagchromatografie. Bron: Gabriel Bolívar. Er zijn verschillende soorten chromatografieën, maar de eenvoudigste, die wordt uitgelegd in de scholen of pre -universitaire cursussen, is die van het papier, wiens principe dezelfde is als die is ontwikkeld op een fijne laag van een absorberend materiaal (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicagel (gewoonlijk silicium )).
De bovenste afbeelding laat zien dat in een beker, vol water of een specifiek oplosmiddel, een papier wordt geplaatst dat een referentielijn is gemarkeerd met druppels of punten van drie geselecteerde pigmenten (oranje, paars en groen). De beker blijft gesloten zodat de druk constant is en verzadigt van de oplosmiddeldampen.
Vervolgens begint de vloeistof door het papier te stijgen en de pigmenten te slepen. De pigment-pale interacties zijn niet allemaal hetzelfde: sommige zijn sterker en andere zwakker. Hoe meer affiniteit het pigment voelt voor het papier, hoe minder het door het papier zal stijgen met betrekking tot de lijn die aanvankelijk was gemarkeerd.
Kan u van dienst zijn: snelheid constantBijvoorbeeld: het rode pigment is degene die minder affiniteit voelt voor het oplosmiddel, terwijl het geel nauwelijks is opgestegen omdat het papier het meer behoudt. Er wordt dan gezegd dat het oplosmiddel de mobiele fase is, en het papier de stationaire fase.
- Fractionele kristallisatie
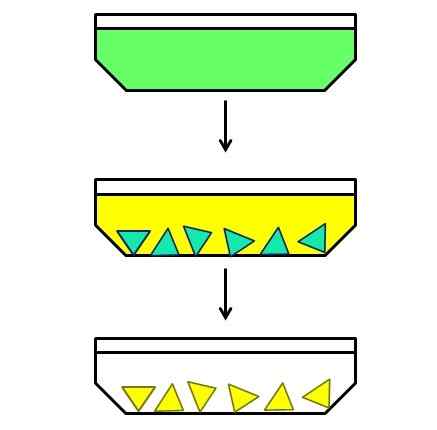 Illustratief voorbeeld van fractionele kristallisatie. Bron: Gabriel Bolívar.
Illustratief voorbeeld van fractionele kristallisatie. Bron: Gabriel Bolívar. En ten slotte heb je fractionele kristallisatie. Deze methode kan misschien als een hybride catalogiseren, omdat deze begint vanuit een homogeen mengsel om een heterogeen te beëindigen. Stel bijvoorbeeld dat er een oplossing is waarin een groene vaste stof is opgelost (superieure afbeelding).
Groene deeltjes zijn te klein om handmatig of mechanisch te scheiden. Het is ook dat de groene vaste stof een mengsel is van twee componenten en geen enkele verbinding van deze kleur.
Dan wordt een oplossing ervan verwarmd en in rust achtergelaten tijdens het afkoelen. Het blijkt dat de twee componenten, hoewel zeer gerelateerd aan elkaar, hun oplosmiddel oplosmiddel enigszins anders zijn; Daarom zal een van de twee eerst beginnen te kristalliseren en vervolgens de andere.
De groenblauwe component (in het midden van de afbeelding) is de eerste die kristalliseert, terwijl de gele component nog steeds is opgelost. Omdat ze groenblauwe kristallen zijn, zijn ze heet voordat gele kristallen verschijnen. Dan, naarmate het oplosmiddel iets meer afkoelt, kristalliseert de geel en wordt een andere filtratie gemaakt.
Thema's van belangstelling
Mengselscheidingsmethoden.
Scheidingsmethoden van heterogene mengsels.
Mengsels: componenten en typen.
Homogene mengsels.
Heterogene mengsels.
Referenties
- Whitten, Davis, Peck & Stanley. (2008). Scheikunde. (8e ed.)). Cengage leren.
- Chelsea Schuyler. (2019). Chromatografie, destillion en filterion: methoden voor het scheiden van mengsels. Studie. Hersteld van: studie.com
- CK-12 Foundation. (16 oktober 2019). Methoden voor het scheiden van mengsels. Chemistry Libhethexts. Hersteld van: chem.Librhetxts.borg
- Goede wetenschap. (2019). Scheiding van mengsels. Hersteld van: GoodScience.com.Au
- Clark Jim. (2007). Dunne laagchromatografie. Hersteld van: chemguide.co.Uk
- « Beloofde (PM) structuur, eigenschappen, verkrijgen, gebruik
- Metalinguïstische functiekarakteristieken, functies en voorbeelden »

