Metalen
- 2346
- 234
- Ernesto McKenzie
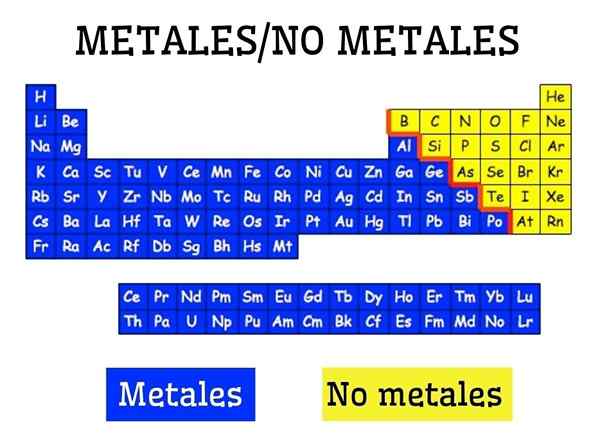
 Metalen en niet -metalen in het periodiek systeem van de elementen
Metalen en niet -metalen in het periodiek systeem van de elementen Wat zijn metalen?
Metalen worden gevormd door een groep elementen die zich aan de linkerkant bevinden, met uitzondering van de niet -metalen waterstof, van het periodiek systeem. Metalen vormen ongeveer 75 % van de chemische elementen, dus er kan worden gezegd dat veel van de natuur metaalachtig is.
De metalen die de mens aanvankelijk in de prehistorie heeft vervolgd, waren de volgende: goud, zilver, koper, tin, lood en ijzer. Dit was te wijten aan het feit dat ze native waren of het gemak van hun verwerking om hulpprogramma's uit te voeren objecten.
Het lijkt een kwestie van magie die van veel rotsen en mineralen glanzende en zilveren lichamen kan worden geëxtraheerd (met bepaalde belangrijke en uitstekende uitzonderingen). Dat is het geval van bauxiet en aluminium, wiens klei rockt dit metaal gereduceerd in platen of zilveren papieren wordt verkregen.
Metalen zijn het kader van industrieën; Hun bedrading, reactoren, eenheden, containers, allemaal op een of andere manier zijn samengesteld uit metalen en hun legeringen.
Met metalen werden de eerste munten, wapens, gereedschappen, pantser gemaakt en vervolgens gebruikt in voertuigfabrikanten, fietsen, schepen, vliegtuigen, computers, onder andere onmisbare objecten in het moderne leven.
Geschiedenis
Kopertijdperk
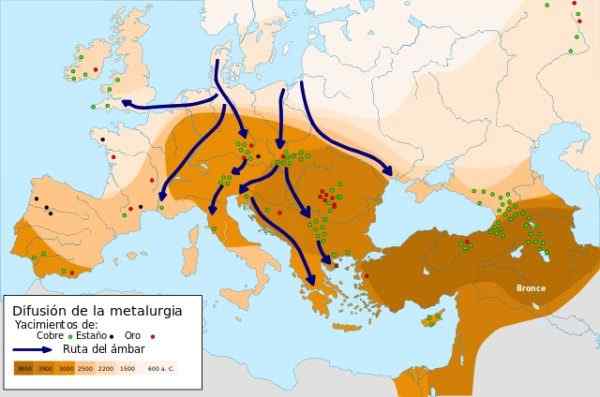 Metallurgie -uitbreiding - Bron: metallurgische diffusie.SVG onder de Creative Commons attributie-compartyrigual 4 licentie 4.0 internationaal
Metallurgie -uitbreiding - Bron: metallurgische diffusie.SVG onder de Creative Commons attributie-compartyrigual 4 licentie 4.0 internationaal In 9000 A.C. De eerste metalen objecten van koper gesmeed in het Nabije Oosten werden uitgewerkt, toen de man ontdekte dat toen het koper hamerd was, hij zijn sterkte en weerstand verhoogde, met behulp van de productie van messen. Dit is het tijdperk van koper.
Er werd ontdekt dat koper kon worden verkregen door het verwarmen van blauwe mineralen, zoals de Corvellita en de Malachiet (4000-3000 tot.C.)).
De calcolithische periode is een tijdsperiode die voorafgaat aan de bronstijd, overeenkomend met 5000-3000 tot.C. De man begon te experimenteren met de fusie en gieterij van koper, om koper te verkrijgen van koperoxide.
Bronstijd (3000-1500 a.C.))
 Bronstijd Materialen - Bron: Gaguilella onder de Creative Commons Attribution -Shareigual 4 License 4.0 internationaal.
Bronstijd Materialen - Bron: Gaguilella onder de Creative Commons Attribution -Shareigual 4 License 4.0 internationaal. De man begon per ongeluk de uitwerking van legeringen, aanvankelijk van koper en arseen, en vervolgens met koper en tin om brons te verkrijgen in het nabije oosten.
Bronze artikelen, die overeenkomen met deze tijd, hadden 87 % koper, 11 % tin en kleine hoeveelheden ijzer, arseen, nikkel, lood en antimoon.
IJzertijd (700 a.C.))
De man gebruikte zijn ervaring in de productie van vervalst koper voor de productie van smeedijzer in het Nabije Oosten. In dezelfde periode was er de granulatie van Etrusco -stof, Italië.
De eerste bekende staalproductie, een ijzer- en koolstoflegering, manifesteerde zich in metalen stukken in een archeologische plaats in Anatolië (1800 tot.C.))
Kan u van dienst zijn: Gravimetrie: Gravimetrische analyse, methoden, gebruik en voorbeeldenTegen 1122 D.C., Op een onbekende datum en plaats wordt gietijzer geïntroduceerd. In 1440 D.C. Beijing's Great Bell wordt geproduceerd, China. Bijna drie eeuwen later, in 1709 D.C., Gietijzer wordt geproduceerd met cola als brandbaar materiaal.
In 1779 werd gietijzer in Engeland gebruikt als architectonisch materiaal. In 1855 gebruikte Henry Bessenir arrabio als grondstof om zacht staal te verkrijgen. Het Engelse Clark and Wood (1872) patent een legering, momenteel beschouwd als roestvrij staal.
Fysieke eigenschappen van metalen
 Het brons van deze oude toeters toont het nut van metalen voor sier- of religieuze doeleinden. Bron: Pxhere.
Het brons van deze oude toeters toont het nut van metalen voor sier- of religieuze doeleinden. Bron: Pxhere. Onder enkele fysieke eigenschappen van metalen hebben we:
-Metalen zijn briljant en kunnen het licht weerspiegelen.
-Over het algemeen zijn ze goede geleiders van elektriciteit en warmte.
-Ze hebben hoge fusie en kookpunten.
-Ze zijn kneedbaar, dat wil zeggen, ze kunnen worden gehamerd om lage dikke vellen te produceren.

-Ze zijn ductiel, met hen kunt u draden of vezels met zeer weinig diameter produceren.
-Ze worden gepresenteerd in een vaste toestand, met uitzondering van kwik dat bij kamertemperatuur zich in vloeibare toestand bevindt, en het gallium, dat net smelt door in de handen in de handen te strakker worden. In de volgende afbeelding kunt u een kwikcontainer zien:

-Het zijn ondoorzichtige lichamen, hun dunne vellen worden niet door het licht gekruist.
-Ze hebben grote hardheid, behalve natrium en kalium dat door een mes kan worden gesneden.
-Ze hebben een hoge dichtheid, zijnde het osmium en het iridium van de hoogste, en het lithium van de laagste dichtheid.
Chemische eigenschappen van metalen
Onder enkele van de chemische eigenschappen van metalen die we hebben:
-Ze hebben de neiging elektronen te verliezen en metalen kationen te vormen, mN+, waarbij N het oxidatienummer aangeeft, dat alleen voor alkalische en alkalistische metalen samenvalt met zijn valentienummer.
-De elektronegativiteiten zijn laag.
-Ze lopen en ervaren oxidatieschade.
-Ze vormen basisoxiden bij het reageren met zuurstof. Deze oxiden in combinatie met water vormen metaalhydroxiden. Metaaloxiden reageren met zuren om zouten en water te vormen.
-Ze zijn goed reductiemiddelen, omdat ze hun elektronen opleveren.
Soorten metalen
Metalen worden geclassificeerd als de volgende: alkalisch, alkalisch-trial, post-transitieve, overgangs- en zogenaamde zeldzame aardes.
Alkalimetalen

Ze vinden zich meestal niet vrij van aard omdat ze gemakkelijk oxideren. Een suborbitale s hebben1 In zijn externe orbitale laag, dus ze hebben een oxidatietoestand +1. Het zijn metalen die exotherma reageren met water en sterk verminderen.
Alkaline-térreos metalen
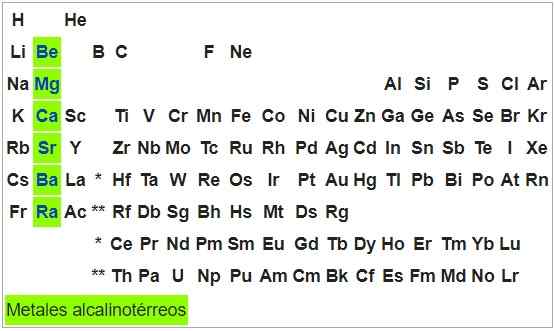
Het zijn kneedbare en ductiele metalen. De atomen van de elementen van deze groep hebben een S -configuratie2, Zodat ze twee elektronen kunnen opleveren en hun oxidatiestatus is +2. Met uitzondering van beryllium zijn ze oxideerbaar voor blootstelling aan lucht.
Kan u van dienst zijn: koolstof AlotropenPosttransitionale metalen
Het zijn metalen van het SO -gekalde P -blok, gelegen tussen overgangsmetalen en metalloïden in het periodiek systeem.
De elementen van groep 3 hebben oxidatietoestanden +1 en +3 als de meest voorkomende, hoewel aluminium alleen de oxidatietoestand +3 presenteert. Het maakt ook deel uit van de post -transitionale metalen in groepen 14 en 15.
Overgangsmetalen D
Ze vormen een groep tussen de basisvormende elementen en zuur -formators. Atomische orbitalen D en F zijn onvolledig en worden gevuld. Hoewel de term overgangsmetalen verwijst naar overgangsmetalen D.
Overgangsmetalen hebben meer dan één oxidatietoestand. Ze hebben fusie- en kookpunten hoger dan andere metaalgroepen. Transition Metals is een zeer heterogene metaalgroep die onder andere bestaat uit ijzer, chroom, zilver, enz.
Zeldzame aarde
 Zeldzame Earth Mineral
Zeldzame Earth Mineral Deze groep metalen bestaat uit de elementen Scandio en Ititrio en de elementen van de reeks lantaniden en actiniden. De term 'zeldzame aarde' verwijst naar het feit dat ze niet in de natuur in pure toestanden worden gevonden en kunnen verbonden zijn door zuren.
Gebruik/toepassingen van metalen
Alkalimetalen
Lithium wordt gebruikt als warmteoverdrachtsmiddelen in sommige kernreactoren. Het wordt gebruikt in sommige droge batterijen en accumulatoren van weinig gewicht. Chloride en lithiumbromide zijn hygroscopische verbindingen die worden gebruikt bij industriële drogen en airconditioningprocessen.
Natrium wordt gebruikt in metaalmetallurgie, zoals titanium en zirkonium. Het wordt gebruikt in openbare verlichting in natriumbooglampen. Natriumchloride (NaCl) wordt gebruikt als voedselsmaak en vleesbehoud.
Alkalineter metalen
Magnesium werd gebruikt in fotografie als flitslicht en vuurwerk. Barium is een onderdeel van legeringen die worden gebruikt in bougies vanwege het gemak van het element om elektronen uit te stoten. Bariumzouten worden gebruikt om de schade te beperken die worden veroorzaakt door x -reeks in maagdarmkanaalplaten.
Calcium wordt gebruikt om onzuiverheden te elimineren die zijn opgelost in gesmolten metalen en bij de eliminatie van restgassen in vacuümbuizen. Het maakt deel uit van het gips, materiaal dat wordt gebruikt in de constructie en bij de behandeling van botbreuken.
Posttransitionale metalen
Aluminium omdat het een licht metaal is, wordt gebruikt bij de constructie van vliegtuigen en vaten. Het wordt ook gebruikt bij de uitwerking van talloze keukengerei. Het wordt gebruikt als grondstof bij de productie van deodorants die het zweten beperken.
Kan u van dienst zijn: percentageoplossingenGallium wordt gebruikt in transistoren en thermometers voor hoge temperaturen. De isotoop 67GA wordt in de geneeskunde gebruikt bij de behandeling van sommige melanomen. Lood wordt gebruikt bij de constructie van batterijen en in bescherming tegen ioniserende straling.
Overgangsmetalen
Koper wordt gebruikt in watervoorzieningsleidingen, in koelkasten en airconditiesystemen. Het wordt ook gebruikt als onderdeel van het hitte -dissipatiemechanisme van de computers. Het wordt gebruikt bij de geleiding van elektrische stroom, in elektromagneten en in de kleuring van glas.
Het nikkel wordt gebruikt bij de uitwerking van roestvrij staal, evenals gitaarreeksen en oplaadbare batterijen. Het wordt ook gebruikt in galvanoplastiek in metaalbescherming. Het wordt gebruikt in legeringen gevonden in delen van voertuigen, zoals kleppen, lagers en remmen.
Het nikkel wordt al lang gebruikt in de uitwerking van munten.
Zink wordt gebruikt bij corrosiemetaalbescherming, in koperen productie. Zinkoxide en zinksulfaat worden gebruikt bij de vervaardiging van platen die worden gebruikt in daken, goten en regenpijpen.
Chroom wordt gebruikt bij de bescherming van metaalcorrosiebescherming en levert glans. Het wordt gebruikt als een katalysator in de ammoniaksynthesereactie (NH3)). Chroomoxide wordt gebruikt in houtbeveiliging.
Zeldzame aarde
De Scandio wordt gebruikt in aluminiumaluminium voor ruimtevaartcomponenten. Het is een additief in kwikdamplampen.
De lantano wordt gebruikt in hoge breking en alkalis -resistent glas. Bovendien wordt het gebruikt bij de productie van camera's en als katalytische katalysatorvloeistoffen voor olieraffinaderijen.
Cerio wordt gebruikt als chemisch middel. Bovendien wordt het gebruikt voor het aanbod van een geel glas en keramische kleuring, evenals katalysator voor zelfwerkende ovens.
Voorbeelden van metaalelementen
Alkalisch
Natrium (NA), kalium (k), cesio (CS), lithium (Li) en rubidium (ru).
Alkalische terreos
Beryllium (be), magnesium (mg), calcium (Ca), strontium (MR), barium (BA) en radio (ra).
Posttransitief
Aluminium (AL), Gallium (GA), Indian (in), Talio (TL), Tin (Sn) en Lead (PB).
Overgangs-
Titanium (Ti), vanadium (V), Chrome (CR), Mangaan (MN), IJzer (geloof), Cobalt (CO), Nikkel (Ni), koper (CUINC), zink (Zn), zirkonium (ZR), Niobio (NB), Molybdeen (MO), Paladio (PD), Silver (Ag), Volframium (W), Renio (RE), Osmio (OS), Iridido (IR),
Platina (PT), goud (AU) en Mercury (Hg).
Zeldzame aarde
Scandio (SC), Itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodymium (ND), Samarium (SM), Europio (EU), Gadolinio (GD), Holmio (ho), Erbio (ER), Tulio (TM), iterbio (YB) en Luthacio (Lu).
Referenties
- Whitten, Davis, Peck & Stanley. (2008). Scheikunde. (8e ed.)). Cengage leren.
- Shiver & Atkins. (2008). Anorganische scheikunde. (Vierde druk). MC Graw Hill.
- Helmestine, Anne Marie, pH.D. (5 oktober 2019). Metalen versus niet -metalen. Hersteld van: Thoughtco.com
- Metalen en hun eigenschappen-fysiek en chemisch. [PDF]. Hersteld van: csun.Edu
- Jonathan -meester. (2019). 18 verschillende soorten metaal (feiten en gebruik). Hersteld van: Makeitfrommetal.com

