Dimethylanylinestructuur, eigenschappen, synthese, gebruik
- 2597
- 371
- Lonnie Rohan
De dimethylanyline o Dimetilfenyllamine is een organische verbinding die wordt gevormd door een benzeenring met een aminogroep vervangen door twee methylgroepen. De chemische formule is c8HelfN.
Het is ook bekend als N, N-dimethylanyline, omdat het een derivaat is van Anylin waarin de aminogroephydrogenen worden vervangen door twee methylgroepen. Dit maakt het een tertiaire amine.
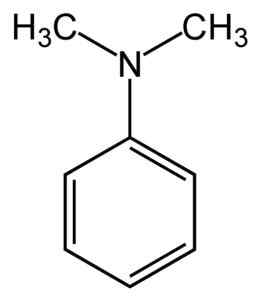 Structuur van N, N-dimethylanyline. Geen machine-leesbare auteur verstrekt. Mysid nam aan (op basis van copyrightclaims). [CC BY-SA 3.0 (http: // creativeCommons.Org/licenties/by-sa/3.0/]]. Bron: Wikipedia Commons.
Structuur van N, N-dimethylanyline. Geen machine-leesbare auteur verstrekt. Mysid nam aan (op basis van copyrightclaims). [CC BY-SA 3.0 (http: // creativeCommons.Org/licenties/by-sa/3.0/]]. Bron: Wikipedia Commons. N, N-dimethylanyline is een lichtgeel tot bruine olieachtige vloeistof met de karakteristieke geur van amines. Het is een basisverbinding en reageert met stikstofzuur die een nitrosocompot vormt. Bij blootstelling aan de lucht wordt het bruin.
Het wordt gebruikt bij de vervaardiging van kleurstoffen voor schilderijen. Het wordt ook gebruikt als een activator van polymerisatiekatalysatoren en in mengsels die worden gebruikt voor beeldopname. Op zijn beurt is het gebruikt bij de synthese van antibacteriële verbindingen of antibiotica als bepaalde penicilline -afgeleide cefalosporines. N, N-dimethylanyline is ook een basis voor het verkrijgen van andere chemische verbindingen.
Het is een brandbare vloeistof en wanneer het wordt verwarmd totdat de ontleding giftige dampen uitzendt. De acute blootstelling van de mens aan het N, N-dimethylanyline kan leiden tot negatieve effecten zoals hoofdpijn, duizeligheid, afname van de zuurstof van het bloed en de huidkleur, onder andere symptomen.
[TOC]
Structuur
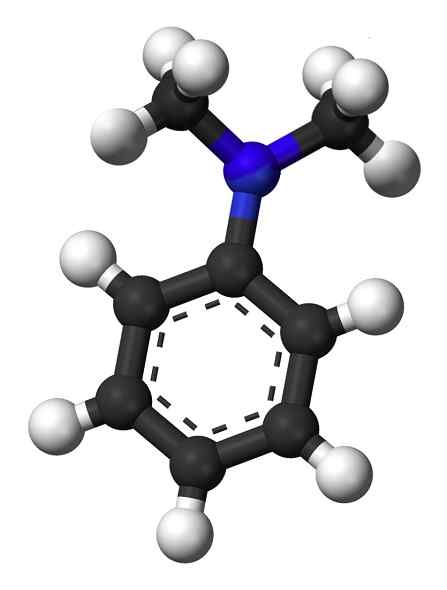
De volgende figuur toont de ruimtelijke structuur van het N, N-dimethylanyline:
 Ruimtelijke structuur van N, N-dimethylanyline. Esquilo [Public Domain]. Bron: Wikipedia Commons.
Ruimtelijke structuur van N, N-dimethylanyline. Esquilo [Public Domain]. Bron: Wikipedia Commons. Nomenclatuur
- N, N-dimethylanyline
- Dimethylanyline
- Dimethylfenyllamine
- N, N-Dimethyl Bencenamine
N wordt in de naam geplaatst om aan te geven dat de twee methylgroepen (-CH3) zijn bevestigd aan stikstof (N) en niet aan de Benncénico -ring.
Eigenschappen
Fysieke staat
Bleek tot bruine vloeistof.
Molecuulgewicht
121.18 g/mol.
Kan u van dienst zijn: anion: training, kenmerken en typenSmeltpunt
3 ºC.
Kookpunt
194 ºC.
Flitslicht
63 ºC (methode gesloten beker). Het is de minimumtemperatuur waarbij dampen kunnen worden ingeschakeld als er een vlam wordt doorgegeven.
Dampdruk
0,70 mm Hg bij 25 ºC.
Zelf -richtingtemperatuur
371 ºC. Het is de minimumtemperatuur bij spontaan brandende atmosferische druk, zonder een externe bron van warmte of vlam.
Dikte
0,9537 g/cm3 bij 20 ºC.
Brekingsindex
1.5582 tot 20 ºC.
Oplosbaarheid
In water is het heel weinig oplosbaar: 1.454 mg/l A 25 ºC.
Vrij oplosbaar in alcohol, chloroform en ether. Oplosbaar in aceton, benzeen en geoxygeneerde en gechloreerde oplosmiddelen.
Basiciteit constant
KB 11.7, dat het gemak aangeeft waarmee deze verbinding een waterstofion van water accepteert.
Chemische eigenschappen
N, N-dimethylanyline is een basisverbinding. Reageert met azijnzuur om acetaat van N, N-Dimetilanilinio te geven.
De -n -groep (kies3))2 van de N is N-dimethylanyline een krachtige aromatische substitutieactivator in de positie voor van de benzeenring.
Reageert met natriumnitriet (nano2) In aanwezigheid van zoutzuur (HCl) die p-nitroso-N, N-dimethylanyline vormt. Ook met stikstofzuur genereert dezelfde samengestelde nitrosado in positie voor.
Bij het reageren van de n, n-dimetilaniline met het benzezoniumchloride, in een zacht zuur medium, is er een azocompled ar-n = n-ar 'type, waarbij AR een aromatische groep is. De moleculen met azo -groepen zijn sterk gekleurde verbindingen.
Risico's
Wanneer verwarmd tot zijn ontleding zendt zeer giftige dampen van stikstofoxiden NO uitX.
Het is een brandbare vloeistof.
Het ontleedt langzaam in water dat wordt blootgesteld aan zonlicht. Het is niet biologisch afgebroken.
Het is ontluchting van natte grond en wateroppervlakken. Verdamp niet droge grond en beweeg hier doorheen. Accumuleert niet in vissen.
Kan u van dienst zijn: ijzersulfide (ii): eigenschappen, risico's en gebruikKan worden geabsorbeerd door de huid. Het wordt ook snel geabsorbeerd door inademing. De blootstelling van de mens aan N, N-dimethylanyline kan het zuurstofgehalte van het bloed verminderen, wat resulteert in een blauwachtige huidskleur.
Acute inademing van deze verbinding kan leiden tot negatieve effecten voor het centrale zenuwstelsel en de bloedsomloop, met hoofdpijn, cyanose en duizeligheid.
Synthese
Het kan op verschillende manieren gebeuren:
- Van aniline en methanol onder druk in aanwezigheid van zure katalysatoren, zoals h2SW4. Sulfaat wordt verkregen, wat de basis wordt door natriumhydroxide toe te voegen.
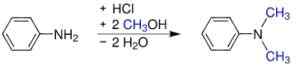 S Synthese, N-dimethylanyline. Werderkli - eigen werk. Publiek domein. Bron: Wikipedia Commons.
S Synthese, N-dimethylanyline. Werderkli - eigen werk. Publiek domein. Bron: Wikipedia Commons. - Het passeren van een anilinedamp en dimethylether op geactiveerd aluminiumoxide.
- Een mengsel van aniline, aniliniumchloride en methanol verwarmen onder druk en vervolgens destilleren.
Toepassingen
In de kleurindustrie
Voor het eigendom van reageren met het Bencenodiazonium-chloride dat azocompiestos vormt, wordt het N-dimethylanyline gebruikt als intermediair in kleurproductie.
Het is grondstof in de synthese van de kleurstoffen van de methylvioletfamilie.
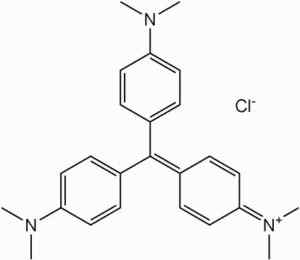 Methylvioletkleur. Geen machine-leesbare auteur verstrekt. Shaddack veronderstelde (op basis van auteursrechtclaims). [Publiek domein]. Bron: Wikipedia Commons
Methylvioletkleur. Geen machine-leesbare auteur verstrekt. Shaddack veronderstelde (op basis van auteursrechtclaims). [Publiek domein]. Bron: Wikipedia Commons Bij de vervaardiging van fotolibele mengsels
Het N, N-dimethylanyline maakt deel uit van een fotocibeerbaar mengsel dat de genezingsreactie ervaart als gevolg van een hoge gevoeligheid voor zichtbaar licht of close infrarood, zodat het kan worden gebruikt voor het opnemen van afbeeldingen of fotorestonerende materialen.
N, N-dimethylanyline is een van de componenten van het mengsel die het bewustzijn van golflengten veroorzaken, zodat de samenstelling is genezen met lage energie-golflengte licht.
Het kan u van dienst zijn: benzeenderivatenNaar schatting is de functie van het N, N-dimethylanyline waarschijnlijk om de beëindigingsreactie van radicale polymerisatie veroorzaakt door zuurstof te onderdrukken.
In de productie van glasvezel
N, N-dimethylanyline wordt gebruikt als een katalytische tarischer in bepaalde fiberglasharsen.
In antibiotica -synthese
N, N-dimethylanyline neemt deel aan de synthese van cefalosporines op basis van penicillines.
Penicillinesulfoxiden worden omgezet in cefemes wanneer verwarmd in aanwezigheid van basiskatalysatoren zoals N, N-dimethylanyline.
Deze cefalosporines vertonen antibacteriële activiteit tegen grampositieve en gram-negatieve organismen, evenals tegen penicilline-resistente staphylococci.
 Antibiotica. Alina Kuptsova. Bron: Pixabay.
Antibiotica. Alina Kuptsova. Bron: Pixabay. Er moet echter worden opgemerkt dat N, N-DimethylanyLine in die antibiotica blijft als onzuiverheid.
Op chemische reacties
N, N-dimethylanyline wordt gebruikt bij de activering van olefinepolymerisatiekatalysatoren.
Het wordt samen met pentafluorofenol gebruikt (c6F5Oh) waarmee de ionische verbinding vormt [hnphme2]+[H (OC6F5))2]-. Deze ionische verbinding heeft een of twee actieve protonen die de katalysator activeren op basis van een overgangsmetaal.
Bovendien is N-dimethylanyline in harsenproductie gebruikt als een polymerisatie-versneller of promotor voor polyesterharsen. De actie ervan genereert een snelle uitharding van de hars.
In verschillende toepassingen
Het wordt gebruikt bij de synthese van andere chemische verbindingen, bijvoorbeeld vanilline, en als intermediair voor farmaceutische geneesmiddelen.
Het wordt ook gebruikt als een oplosmiddel, als een alkyleringsmiddel, als stabilisator en om schilderijen en coatings te produceren.
Referenties
- S. Nationale bibliotheek van geneeskunde. (2019). N, N-dimethylaniline. Hersteld van: pubchem.NCBI.NLM.NIH.Gov
- Morrison, r.T. en Boyd, r.N. (2002). Organische chemie. 6e editie. Prentice-Hall.
- (2000). N, N-dimethylaniline. Samenvatting. Opgehaald van EPA.Gov
- Zanaboni, p. (1966). Onverzadigde polyester harsachtige samenstelling HAVH -stabiliteit en snelle uitharding bij lage temperaturen met behulp van een mengsel van dimethylanil, trenhanolamine en difenylamine. OF.S. Octrooi nee. 3.236.915. 22 februari 1966.
- Nudelman, een. en McCaully, r.J. (1977). Proces voor de herschikking van penicillines voor cefalosporines en tussenliggende compounders daarvan. OF.S. Octrooi nee. 4.010,156. 1 maart 1977.
- Kouji Inaishi (2001). Fotociabele compositie. OF.S. Octrooi nee. 6.171.759 B1. 9 januari 2001.
- Luo, L. et al. (2012). Ionisch Bransted Acid. OF.S. Octrooi nee. 8.088.952 B2. 3 januari 2012.
- « Rodio geschiedenis, eigenschappen, structuur, gebruik, risico's
- Acute geluiden kenmerken en voorbeelden »

