Natriumbisulfiet (NAHSO3) structuur, eigenschappen, gebruik, verkrijgen
- 4177
- 436
- Alton D'Amore
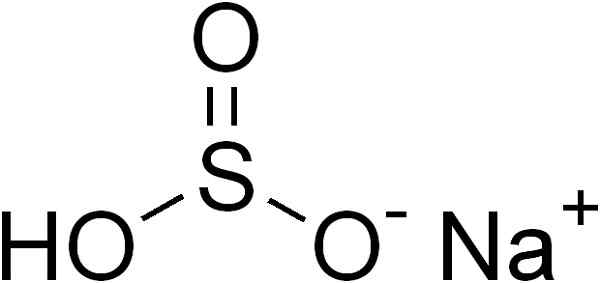
Hij natriumbisulfiet Het is een anorganische vaste stof gevormd door een ionen natrium na+ en een HSO bisulfiet -ion3-. De chemische formule is nahso3. Het is een kristallijne witte vaste stof en voor zijn antioxiderende eigenschappen wordt veel gebruikt als voedselconservatief (bijvoorbeeld in sommige jam).
De nahso3 Het is een reducerende chemische verbinding, die het tegenovergestelde is van oxideren, en om deze reden fungeert het als een antioxidant in veel van zijn toepassingen, zoals eetbare producten, omdat het zijn verslechtering voorkomt.
 Sommige commerciële jam bevatten Nahso natriumbisulfiet3. Auteur: OpenClipart-Vectors. Bron: Pixabay.
Sommige commerciële jam bevatten Nahso natriumbisulfiet3. Auteur: OpenClipart-Vectors. Bron: Pixabay. Dit gebruik is echter in twijfel getrokken omdat gevallen van astma bij mensen zijn gemeld nadat ze voedingsmiddelen hebben gegeten die natriumbisulfiet bevatten. Er wordt zelfs gezegd dat het vitamine B1 hiervan vernietigt.
Internationale gezondheidsorganisaties hebben hun gebruik beperkt tot microcontities in voedsel.
Natriumbisulfiet heeft echter vele andere toepassingen, zoals bij het verkrijgen van jodium, als anti -infectie, om weefsels te bleken, voor de spijsvertering van hout tijdens het bereiden van papieren pulp, als een ontsmettingsmiddel van bier- en wijnvaten, enz.
[TOC]
Chemische structuur
Natriumbisulfiet wordt gevormd door een natrium na kation+ en een HSO bisulfietanion3-.
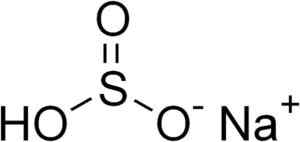 Chemische structuur van natriumbisulfiet3. Edgar181 [Public Domain]. Bron: Wikimedia Commons.
Chemische structuur van natriumbisulfiet3. Edgar181 [Public Domain]. Bron: Wikimedia Commons. In waterige oplossingen vormt bisulfiet 4 soorten. In verdunde oplossing is er een evenwicht tussen de onderstaande structuren:
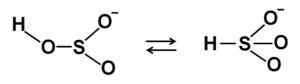 Hso bisulfiet ionstructuren3- In verdunde waterige oplossing. Auteur: Marilú Stea.
Hso bisulfiet ionstructuren3- In verdunde waterige oplossing. Auteur: Marilú Stea. Wanneer de concentratie toeneemt, interageren twee bisulfietmoleculen met elkaar die de pyrosulfiet -ionen vormen2OF52-:
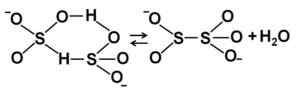 Bisulfiet -ionstructuren in geconcentreerde waterige oplossing. Auteur: Marilú Stea.
Bisulfiet -ionstructuren in geconcentreerde waterige oplossing. Auteur: Marilú Stea. Nomenclatuur
-Natriumbisulfiet
-Natriumhydrogenosulfiet
-Natriumhydrosulfiet.
Eigenschappen
Fysieke staat
Kristallijne witte vaste stof.
Molecuulgewicht
104.06 g/mol
Smeltpunt
Het ontleedt.
Dikte
1,48 g/cm3 bij 20 ºC.
Oplosbaarheid
Wateroplosbaar: 29 g/100 g water.
pH
De oplossingen zijn zuur, met een pH tussen 2,5 en 5,5.
Chemische eigenschappen
In waterige oplossing natriumbisulfiet3 wordt gescheiden in zijn ionen: het natriumkation na+ en het HSO bisulfiet -anion3-.
Als natriumbisulfiet wordt blootgesteld aan lucht verliest sommigen zo2 en oxideert langzaam sulfaat2SW4.
Het kan u van dienst zijn: Gallischzuur: structuur, eigenschappen, verkrijgen, gebruikAls het wordt verwarmd tot zijn ontleding zwaveloxiden en natriummonoxide uitzendt.
Het is een reductiemiddel, dat het tegenovergestelde is van oxidatiemiddel. En om deze reden kan het zich gedragen als antioxidant.
Het heeft een lichte geur van zwavel. Het is niet ontvlambaar.
Risico's
Nahso natriumbisulfiet3 Het is een sterk leer en weefsel irriterend. Het stof irriteert de ogen, neus en keel. Door inname de maag te irriteren. Grote doses kunnen gewelddadige krampen, diarree, depressie en de dood veroorzaken.
Het is geen brandstof, maar het wordt verwarmd, produceert irritante en giftige gassen.
Het verkrijgen van
Het wordt bereid door een natriumcarbonaatoplossing NA te verzadigen2CO3 Met zwaveldioxide dus2 en kristalliseert in de oplossing.
Toepassingen
In de pulp- en papierindustrie
De nahso3 Het wordt gebruikt bij de vertering van het hout, zodat het dan papier kan worden. Het dient ook als pulp witter.
Het wordt ook gebruikt om chloor te elimineren wanneer de papieren pulp hiermee is gebleekt.
In de voedingsindustrie
Natriumbisulfiet voor zijn reducerende eigendom werkt als een antioxidant.
Het wordt gebruikt als een conserveermiddel in een grote hoeveelheid eten en drinken, inclusief wijn en bier, om de achteruitgang te voorkomen en de smaak te verbeteren.
Het dient om voedsel te bleken, zoals bepaalde eetbare zetmeel.
Het vermindert of voorkomt de verslechtering van voedsel, maakt het mogelijk om het deeg te conditioneren dat wordt gebruikt in gebakken voedsel en serveert om maïskorrels te verzachten tijdens natte slijpen, onder andere toepassingen.
Naast het beheersen van de gisting van wijn en bier, fungeert het als een antisepticum in zijn uitwerking omdat het dient als steriliserend en fungicide in vaten en tanden.
 Wijn- of biervaten worden soms gedesinfecteerd met natriumbisulfiet3. Auteur: Clker-vrije-vector-afbeeldingen. Bron: Pixabay.
Wijn- of biervaten worden soms gedesinfecteerd met natriumbisulfiet3. Auteur: Clker-vrije-vector-afbeeldingen. Bron: Pixabay. In gedroogd fruit is het in concentraties boven 100 ppm (ppm betekent "delen per miljoen"), in veel andere voedingsmiddelen is het in concentraties tussen 10 en 100 ppm, zoals bevroren en droge aardappelen, augurken, sauzen en jam.
 Commercieel ingelegde voedsel bevat vaak Nahso natriumbisulfiet3. Auteur: fotomix. Bron: Pixabay.
Commercieel ingelegde voedsel bevat vaak Nahso natriumbisulfiet3. Auteur: fotomix. Bron: Pixabay. Controverse over het gebruik ervan in voedsel
Er is enige bezorgdheid geweest over de toxische effecten, zowel onmiddellijk als op lange termijn van natriumbisulfiet in voedsel. Er zijn uiteenlopende meningen.
Kan u van dienst zijn: kaliumferrocyanideEr zijn meldingen van bijwerkingen van patiënten met astma, een ademhalingsziekte, na de inname van boodschappen met NAHSO3. Andere bronnen geven aan dat het bisulfiet -ion vitamine B1 of thiamine kan vernietigen.
 Meisje dat een medicijn streeft om astma te verlichten. Auteur: OpenClipart-Vectors. Bron: Pixabay.
Meisje dat een medicijn streeft om astma te verlichten. Auteur: OpenClipart-Vectors. Bron: Pixabay. Bepaalde onderzoekers in 1985 ontdekten echter dat natriumbisulfiet dient om te beschermen tegen chemische middelen, en remt of voorkomt de transformatie van cellen in kanker. De lage doses zijn de beste.
Dit beschermende effect is verklaard op basis van de reducerende of antioxiderende eigenschappen en dat op deze manier vrije radicalen zou kunnen aanvallen.
Aan de andere kant, de Wereldgezondheidsorganisatie, of WHO (voor haar acroniem voor Engels Wereldgezondheidsorganisatie), beveelt aan als een acceptabel niveau van dagelijkse inname van ongeveer 0,7 mg/kg van de persoon.
Dat betekent dat het wordt aanbevolen dat bedrag niet te overschrijden.
De Food and Medicine Administration van de Verenigde Staten, of USFDA (Engels acroniem US Food and Drug Administration), hij classificeerde natriumbisulfiet als "algemeen erkend als verzekering".
In agrarische toepassingen
Gebruikt bij lage concentraties de nahso3 Het dient als een plantengroeiregulator om de fotosynthese te verbeteren en de prestaties van gewassen te bevorderen.
Dit doel is getest in verschillende soorten planten, zoals aardbei- en theeplanten.
 Aardbeienplanten verbeteren hun prestaties met kleine hoeveelheden nahso3 In irrigatiewater. Auteur: Alyssapy. Bron: Pixabay.
Aardbeienplanten verbeteren hun prestaties met kleine hoeveelheden nahso3 In irrigatiewater. Auteur: Alyssapy. Bron: Pixabay. Het is het actieve ingrediënt van veel pesticiden en biociden.
In wateromgevingen kan het ook de transformatie van bepaalde herbiciden naar minder giftige producten versnellen door chloor te elimineren.
Bij het verkrijgen van jodium
De nahso3 Het is de reducerende verbinding die wordt gebruikt om jodinus van natrium naio af te geven3. Dit is een van de manieren om jodium te halen uit bronnen zoals de Chileense nitro of sommige Salinas -wateren.
Na het kristalliseren van het natriumnitraat van de nitraatoplossing van grove chili, is er een NAIO -oplossing3 dat wordt behandeld met natriumbisulfiet3, gratis jodium genereren.
2 NAIO3 + 5 Nahso3 → 3 Nahso4 + NA2SW4 + Je2
In de meubels en houtindustrie
De nahso3 Het is getest om soja -eiwitten te wijzigen en zijn hechteigenschappen te verbeteren met hout met het doel van paste stukken hout van elkaar om te bereiden, bijvoorbeeld agglomeraten, houtkarton of stenen karton, aanrechtvormige, etc. Allemaal voor meubels of boards, onder verschillende toepassingen.
Het kan u van dienst zijn: lithiumhydroxide (liOH) Agglomeraat van splinters of houten overblijfselen. Auteur: Titus Tschardke [Public Domain]. Bron: Wikimedia Commons.
Agglomeraat van splinters of houten overblijfselen. Auteur: Titus Tschardke [Public Domain]. Bron: Wikimedia Commons. Dit wordt gedaan om traditionele lijmen te vervangen op basis van formaldehyde, omdat zowel in hun productieproces als tijdens gebruik de neiging hebben om de atmosfeer vrij te formaliseren, wat een giftige verbinding is.
Natriumbisulfiet verbetert het vaste gehalte van de soja -eiwitlijm en vermindert de viscositeit van deze verbetering ervan, zodat het de poriën van het hout doordringt, waardoor de cohesie met deze en tussen de stukken wordt verhoogd.
Soja -eiwitlijm gemodificeerd met nahso3 Het heeft een goede waterweerstand en uitstekende opslagstabiliteit vanwege de antioxiderende werking van natriumbisulfiet.
Dit bevestigt dat gemodificeerde soja -eiwitlijmen met nahso3 Ze zijn vergelijkbaar met lijmen op basis van formaldehyde en kunnen worden gebruikt in het meubilair en de houtindustrie, die minder vervuilend zijn.
In verschillende toepassingen
Het heeft meerdere toepassingen, meestal gebaseerd op de reducerende eigenschappen (wat het tegenovergestelde is van oxidatiemiddel). Hier zijn enkele toepassingen.
-In fotografie.
-In de lederen leerlooier, om haar uit de huiden te verwijderen.
-Therapeutisch gebruik: anti -onfeilbaar. Het wordt gebruikt als antioxidant in enkele druppels voor -ojos.
-In aardgaswinning door hydraulische breuk.
-Bij vezelkleuring wordt het gebruikt voor het bereiden van baden met warme of koude buizen, om bepaalde kleurstoffen of kleurstoffen op te lossen.
-Als een afname in was of bleken, om wol, zijde en plantenvezels te bleken.
-In chemie -laboratoria om huid- en kledingvlekken te verwijderen. In biochemie -laboratoria als een vloeistofconserveermiddel of oplossingen die in de loop van de tijd kunnen worden verslechterd. Als chemisch reagens.
-Voor rubber latex coagulatie.
-In de cosmetische industrie als antioxidant.
-Ontsmettingsmiddel en bleekmiddel.
-In afvalwaterzuivering om chloor te elimineren die wordt gebruikt in de laatste fase van desinfectie en de wateren te downloaden die al naar het milieu zijn behandeld.
 Natriumbisulfiettank in een afvalwaterzuiveringsinstallatie in Californië, waar het wordt gebruikt om overtollig chloor te elimineren voordat gezuiverde wateren naar de omgeving worden gedownload. Grendelkhan [CC BY-SA 3.0 (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons.
Natriumbisulfiettank in een afvalwaterzuiveringsinstallatie in Californië, waar het wordt gebruikt om overtollig chloor te elimineren voordat gezuiverde wateren naar de omgeving worden gedownload. Grendelkhan [CC BY-SA 3.0 (https: // creativeCommons.Org/licenties/by-sa/3.0)]. Bron: Wikimedia Commons. Referenties
- OF.S. Nationale bibliotheek van geneeskunde. (2019). Natriumbisulfiet. Hersteld van PubChem.NCBI.NLM.NIH.Gov.
- Qi, g. et al. (2013). Adhesie en fysicochemische eigenschappen van Ser -eiwit gemodificeerd door natriumbisulfiet. J Am Oil Chem Soc (2013) 90: 1917-1926. Hersteld van AOC's.Online bibliotheek.Wiley.com.
- Borek, c. et al. (1985). Natriumbisulfiet beschermt tegen radiogogene en chemisch geïnduceerde transformion in hamsterembryo en muis C3H/10T-1/2-cellen. Toxicol Ind Health 1985Sep; 1 (1): 69-74. Hersteld van tijdschriften.Sagepub.com.
- Friedler, E. et al. (2015). Een continue actieve monitoringbenadering om kruisverbindingen tussen drinkwater en effluentverdelingssystemen te identificeren. Environment Monit Assess (2015) 187: 131. Link hersteld.Springer.com.
- Katoen, f. Albert en Wilkinson, Geoffrey. (1980). Geavanceerde anorganische chemie. Vierde druk. John Wiley & Sons.
- Sunnyvale Cleanwater -programma. (2019). Watervervuilingscontrole plant masterplan. Hersteld van SunnyValecleanwater.com.
- Barros Santos, C. (2008). Additieven bij het voeden van de Spanjaarden en de wetgeving die hun autorisatie en gebruik reguleert. Boeken visie. Hersteld uit boeken.Google.co.gaan.

