Alcohol
- 4924
- 1007
- Miss Herman Russel
 Ethanolmolecuul of ethylalcohol. Met licentie
Ethanolmolecuul of ethylalcohol. Met licentie Wat zijn alcoholen?
De Alcohol Het zijn organische verbindingen die worden gekenmerkt door een hydroxylgroep (-OH) te hebben gekoppeld aan een verzadigde koolstof, dat wil zeggen een koolstof die is gekoppeld aan vier atomen door eenvoudige bindingen (zonder dubbele of drievoudige links).
De generieke formule voor deze enorme en veelzijdige familie van verbindingen is ROH. Om in strikt chemische zin als alcohol te worden beschouwd, moet de OH -groep de meest reactieve van de moleculaire structuur zijn. Dit is belangrijk om te bevestigen, tussen verschillende moleculen met OH -groepen, die van hen een alcohol is.
Een van de alcoholen bij uitstek en de bekendste in de populaire cultuur is ethylalcohol, of ethanol, ch3Ch2Oh. Afhankelijk van hun natuurlijke oorsprong, en daarom van hun chemische omgeving, kunnen hun mengsels een onbeperkt spectrum van smaken veroorzaken, sommige, die zelfs positieve veranderingen in de gehemelte vertonen met de loop van de jaren.
Alcoholstructuur
Alcoholen hebben een algemene ROH -formule. De OH -groep is gekoppeld aan de alquilicale groep, wiens structuur varieert van de ene alcohol tot de andere. De unie tussen R en OH is een eenvoudige covalente link, R-OH.
De volgende afbeelding toont drie generieke structuren voor alcoholen, gezien het feit dat het koolstofatoom verzadigd is, dat wil zeggen dat het vier eenvoudige links vormt.
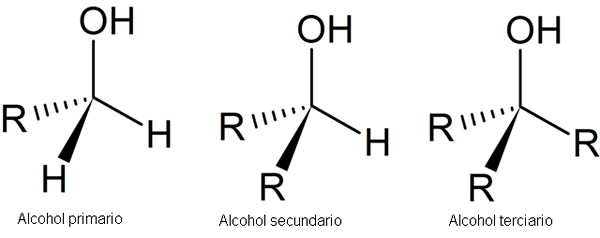 Alcoholstructuur. Bron: Secalinum, Wikimedia Commons
Alcoholstructuur. Bron: Secalinum, Wikimedia Commons Zoals te zien is, kan r elke koolzuurhoudende structuur zijn, zolang het geen meer reactieve substituenten bezit dan de OH -groep.
In het geval van primaire alcohol, 1e, is de OH -groep gekoppeld aan een primaire koolstof. Dit wordt gemakkelijk geverifieerd door op te merken dat het atoom in het midden van de linker tetraëder is gekoppeld aan een r en twee h.
Secundaire alcohol, 2e, is geverifieerd met de koolstof van de tetraëder van het centrum nu gekoppeld aan twee R -groepen en een h.
En ten slotte heb je tertiaire alcohol, 3e, met koolstof gekoppeld aan drie R -groepen.
Amfifiel karakter
Afhankelijk van het type koolstof dat is gekoppeld aan OH, hebt u de classificatie van primaire, secundaire en tertiaire alcoholen. In de tetrahedra waren de structurele verschillen tussen hen al gedetailleerd. Maar alle alcoholen, ongeacht hun structuur, delen iets gemeen.
Het is niet nodig om een structuur aan te pakken om deze op te merken, maar het is voldoende met zijn ROH -chemische formule. De huurgroep is bijna volledig samengesteld.
Aan de andere kant kan de OH -groep waterstofbruggen vormen met de watermoleculen, die daarom hydrofyl zijn, dat wil zeggen, het presenteert een affiniteit voor water. Vervolgens hebben alcoholen een hydrofoob skelet, samen met een hydrofiele groep. Ze zijn tegelijkertijd apolair en polair, wat hetzelfde is als zeggen dat het amfifiele stoffen zijn.
Kan u van dienst zijn: verschillen tussen homogene mengsels en heterogene mengselsR-OH
(Hydrofoob) - (hydrofiel)
Zoals in de volgende sectie zal worden verklaard, definieert het amfifiele karakter van alcoholen enkele van hun chemische eigenschappen.
Structuur van r
De Renta R -groep kan elke structuur hebben, en toch is het belangrijk omdat de alcoholen kunnen worden geclassificeerd.
R kan bijvoorbeeld een open ketting zijn, zoals het geval is bij ethanol of propanol, vertakt, zoals T-butylalcohol (CH3))2Chch2Oh, het kan cyclisch zijn, zoals in het geval van cyclohexanol, of kan een aromatische ring hebben, zoals in benzylalcohol (c6H5) Ch2Oh, of in 3-fenilpropanol (c6H5) Ch2Ch2Ch2Oh.
De R-keten kan zelfs substituenten hebben zoals halogenen of dubbele bindingen, zoals voor alcoholen 2-cellen en 2-stukje-1-ol (CH3Ch2= Chch2OH).
Gezien de structuur van R, wordt de classificatie van alcoholen complex. Daarom is de classificatie op basis van de structuur (1e, 2e en 3e alcohol) eenvoudiger maar minder specifiek, hoewel het voldoende is om de reactiviteit van alcoholen te verklaren.
Fysische en chemische eigenschappen
- Kookpunt: Een van de belangrijkste eigenschappen van alcoholen is dat ze worden geassocieerd door waterstofbruggen. Dankzij dit zijn alcoholen meestal vloeibaar met hoge kookpunten.
- Oplosmiddelcapaciteit: In huizen is het heel gebruikelijk om hun toevlucht te nemen tot het gebruik van isopropylalcohol om een vlek te verwijderen die moeilijk op een oppervlak te verwijderen is. Deze oplosmiddelcapaciteit, zeer nuttig voor chemische synthese, is te wijten aan zijn amfropifilkarakter, eerder uitgelegd. Vetten worden gekenmerkt door hydrofoob te zijn: daarom is het moeilijk om ze met water te verwijderen. In tegenstelling tot water hebben alcoholen echter een hydrofobe deel in hun structuur. De groep Renta R werkt dus in wisselwerking met vetten, terwijl de OH -groep waterstofbruggen vormt met water, waardoor ze worden verplaatst.
- Anfoterisme: Alcoholen kunnen reageren als zuren en basen, dat wil zeggen, het zijn amfotent -stoffen. Dit wordt weergegeven met de volgende twee chemische vergelijkingen:
ROH + H+ => ROH2+
ROH + OH- => Ro-
De Ro- Het is de algemene formule van wat bekend staat als een alcoxide.
Nomenclatuur
Er zijn twee manieren om alcoholen te noemen, waarvan de complexiteit zal afhangen van hun structuur.
Gemeenschappelijke naam
Alcoholen kunnen worden opgeroepen voor hun gemeenschappelijke namen. Om dit te doen, moet de naam van de R -groep bekend zijn, waaraan het einde is toegevoegd en wordt voorafgegaan door het woord 'alcohol'. Bijvoorbeeld cho3Ch2Ch2Oh is propylico alcohol.
Kan u van dienst zijn: heterogeen systeemAndere voorbeelden zijn:
- Ch3OH: methylalcohol.
- (Ch3))2Chch2OH: Isobutylalcohol.
- (Ch3))3COH: Tert-Boutyl Alcohol.
IUPAC -systeem
Wat betreft gemeenschappelijke namen, moet u beginnen met het identificeren van r. Het voordeel van dit systeem is dat het veel preciezer is dan de andere.
A, omdat het een koolstofskelet is, kan het gevolgen hebben of meerdere ketens. De langste keten, die, met meer koolstofatomen, is waaraan de naam van alcohol zal worden toegekend.
De naam van de langste ketting wordt toegevoegd aan de naam van de alkane, de beëindiging 'l' wordt toegevoegd. Dat is de reden waarom Cho3Ch2Oh heet Ethanol (Cho3Ch2- + OH).
Over het algemeen moet oh de minst mogelijke opsomming hebben. Bijvoorbeeld de BRCH2Ch2Ch2(Oh) cho3 Het wordt 4-broom-2-butanol genoemd en niet 1-broom-3-butanol.
Synthese
Alkenes Hydratatie
Het olie -crapatieproces produceert een mengsel van vier of vijf koolstofatomen, die gemakkelijk kunnen scheiden.
Deze alkenen kunnen alcoholen worden door de directe toevoeging van water of door de reactie van het alkeen met zwavelzuur, gevolgd door de toevoeging van het water dat het zuur splitst, afkomstig uit de alcohol.
Oxo -proces
In aanwezigheid van een adequate katalysator reageren alkenen met koolstof en waterstofmonoxide om aldehyden te genereren. Aldehydos kunnen gemakkelijk worden gereduceerd tot alcoholen door een katalytische hydrogeneringsreactie.
Er is vaak een dergelijke synchronisatie van het OXO -proces dat de vermindering van aldehydos bijna gelijktijdig is met hun formatie.
De meest gebruikte katalysator is de decobalto octocarbonil, verkregen door de reactie tussen kobalt en koolmonoxide.
Koolhydraatfermentatie
Koolhydraatfermentatie voor gist is nog steeds van groot belang bij de productie van ethanol en andere alcoholen. Suikers komen van suikerriet of zetmeel verkregen uit verschillende korrels. Om deze reden wordt ethanol ook wel "graanalcohol" genoemd
Toepassingen
Drankjes
- Hoewel het niet de belangrijkste functie van alcoholen is, is de aanwezigheid van ethanol in sommige drankjes een van de meest populaire kennis. Aldus ethanol, product van de gisting van suikerriet, druiven, appel, etc., Het is aanwezig in tal van sociale consumptie -dranken.
Chemisch grondstof
- Methanol wordt gebruikt in de productie van formaldehyde, door zijn katalytische oxidatie. De formaldehyde wordt gebruikt bij de productie van kunststoffen, schilderijen, textiel, explosieven, enz.
- Butanol wordt gebruikt bij de productie van butanoat -butaan, een ester die wordt gebruikt als een smaakstof in de voedingsindustrie en zoetwaren.
- Allyische alcohol wordt gebruikt bij de productie van esters, waaronder het ftalaat van Dialilo en dialilo isftalate, die als monomeren dienen.
- Het fenol wordt gebruikt bij de productie van harsen, nylonproductie, deodorants, cosmetica, enz.
- Lineaire ketenalcoholen van 11-16 koolstofatomen worden gebruikt als tussenpersonen om weekmakers te verkrijgen. Bijvoorbeeld polyvinylchloride.
- De zo -called vetalcoholen worden gebruikt als intermediairs in de synthese van wasmiddelen.
Oplosmiddelen
- Methanol wordt gebruikt als een verfoplosmiddel, evenals 1-butanol en isobutilische alcohol.
- Ethylalcohol wordt gebruikt als een oplosmiddel van veel onoplosbare verbindingen in het water, met behulp van een oplosmiddel in schilderijen, cosmetica, enz.
- Vettige alcoholen worden gebruikt als oplosmiddelen in de textielindustrie, in kleurstoffen, in wasmiddelen en in schilderijen. Isobutanol wordt gebruikt als oplosmiddel in coatingmateriaal, schilderijen en lijmen.
Brandstoffen
- Methanol wordt gebruikt als brandstof in interne en additieve benzinemotoren om de verbranding te verbeteren.
- Ethylalcohol wordt gebruikt in combinatie met fossiele brandstoffen in motorvoertuigen. Daartoe zijn uitgebreide regio's van Brazilië bedoeld voor de teelt van suikerriet voor ethylalcoholproductie. Deze alcohol heeft het voordeel dat het in zijn verbranding alleen koolstofdioxide produceert. Wanneer ethylalcohol wordt verbrand, produceert dit een schone en rookloze vlam, daarom wordt het gebruikt als brandstof in campagnekeukens.
- Gelified alcohol wordt geproduceerd door combinatie van methanol of ethanol met calciumacetaat. Deze alcohol wordt gebruikt als een warmtebron in campagne -kachels, en omdat het morst is het veiliger dan vloeibare alcoholen.
- De zo -gevallen biobutanol wordt gebruikt als transportbrandstof, evenals isopropylische alcohol, hoewel het gebruik ervan niet wordt aanbevolen.
Antiseptica
- 70% concentratie isopropylalcohol wordt gebruikt als een externe antisepticum voor de eliminatie van ziektekiemen en vertraging van de groei, net als ethylalcohol.
Andere gebruiken
- Cyclohexanol en methylciclohexanol worden gebruikt in de textielafwerking, meubels verwerkt en chitamanchas.
Voorbeelden van alcoholen en hun formules
- Methanol (ch3OH).
- 1-propanol (c3H7OH).
- Ethanol (c2H5OH).
- Isobutanol (c4H9OH).
- Isopropanol (c3H8OF).
- Allilic alcohol (c3H6OF).
- Benzylalcohol (c7H8OF).
- Thermisch (c₄h₁₀o).
- Perenol (c5HelfOH).
- 2-butanol (ch3-Ch2-Choh-CH3)).
- Fenol (c6H6OF).
- 2-propanol (ch3-Choh-CH3)).
- Isodecanol (c10H21OH).
- Cetylalcohol (c16H3. 4OF).
- Propargilische alcohol (c3H4OF).
- Tetrahydrofurilische alcohol (c5H10OF2)).
- Cyclohexanol (c6H12OF).
- 2-chlorotanol (c2H5Clo).
- Heptanol (c7H16OF).
- Hexanol (c₆h₁₄o).
Referenties
- Organische chemie. MC Graw Hill.
- Alcohol. Opgehaald uit colapret.cm.Utexas.Edu.

