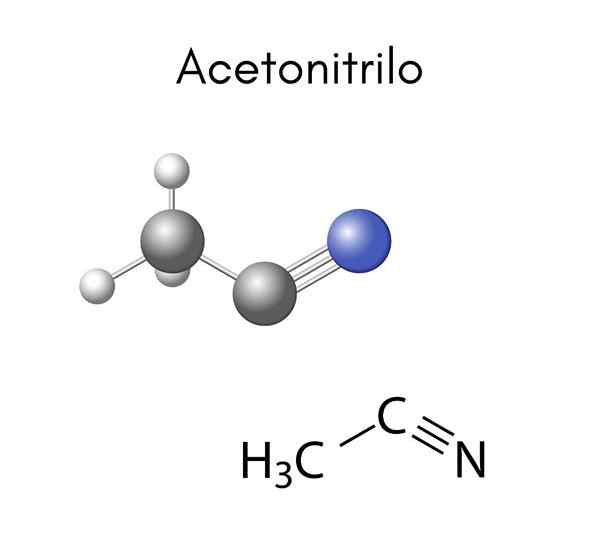
Acetonitril (C2H3N)
- 1739
- 355
- Lonnie Rohan
Wat is acetonitril?
Hij acetonitril Het is een stof van organische oorsprong die alleen uit koolstof, waterstof en stikstof is samengesteld. Deze chemische soort behoort tot de groep nitrillen, waarbij de acetonitril de eenvoudigste structuur is tussen organisch type.
Nitrillen zijn een klasse van chemische verbindingen waarvan de structuur wordt gevormd door een cyanidegroep (CN-) en een radicale ketting (-r). Deze elementen worden weergegeven door de volgende algemene formule: R-C≡N.
Het is bekend dat deze stof voornamelijk wordt ontstaan tijdens de productie van een andere soort genaamd Acrilonitrile (een ander eenvoudig nitril, van moleculaire formule C3H3N, dat wordt gebruikt bij de uitwerking van producten in de textielindustrie) als een bijproduct van hetzelfde.
Bovendien wordt acetonitril beschouwd als een oplosmiddel met gemiddelde polariteitseigenschappen, en daarom wordt het vrij regelmatig gebruikt in RP-HPLC-analyse (acroniem in het Engels voor vloeistofchromatografie met hoge effectiviteit van omgekeerde fase).
Structuur
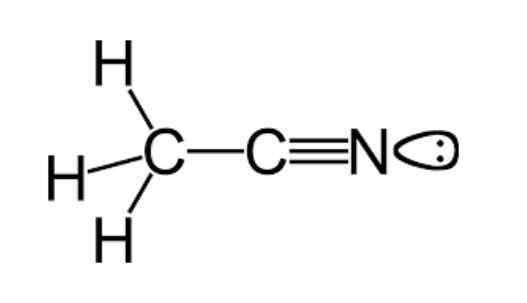
Zoals eerder vermeld, behoort acetonitril tot de functionele groep nitrillen, met een moleculaire formule die gewoonlijk wordt weergegeven als C2H3N, die kan worden waargenomen in de structurele formule geïllustreerd in de bovenste figuur.
Deze afbeelding toont een klasse lob die is bevestigd aan het stikstofatoom, dat het paar ontbrekende elektronen weergeeft dat dit atoom bezit, en die het een groot deel van de reactiviteit en stabiliteitseigenschappen geven die karakteristiek zijn.
Op deze manier manifesteert deze soort een zeer specifiek gedrag vanwege de structurele opstelling, wat zich vertaalt in zwakte om waterstofbindingen te ontvangen en weinig vermogen om elektronen te doneren.
Kan u van dienst zijn: arseen: geschiedenis, structuur, eigenschappen, gebruikEvenzo ontstond deze stof voor het eerst in de tweede helft van de jaren 1840, vervaardigd door de wetenschapper genaamd Jean-Baptiste Dumas, wiens nationaliteit Frans was.
De structurele conformatie van deze stof maakt dit kenmerk van een oplosmiddel van organische aard mogelijk.
Op zijn beurt kan deze eigenschap acetonitril worden gemengd met water, naast een reeks andere oplosmiddelen van organische oorsprong, met uitzondering van koolwaterstoffen of verzadigde koolwaterstofsoorten.
Eigenschappen van acetonitril
Deze verbinding heeft een reeks eigenschappen die het onderscheiden van anderen van dezelfde klasse, die hieronder worden vermeld:
- Het bevindt zich in een toestand van vloeibare aggregatie in standaarddruk- en temperatuuromstandigheden (1 atm en 25 ° C).
- De moleculaire configuratie geeft het een molaire massa of molecuulgewicht van ongeveer 41 g/mol.
- Het wordt beschouwd als de nitril die de eenvoudigste structuur heeft, tussen organische typen.
- Door zijn optische eigenschappen kan het kleurloos zijn in deze vloeibare fase en schijnbare kenmerken, naast het hebben van een aromatische geur.
- Het heeft een ontstekingspunt rond 2 ° C, gelijk aan 35,6 ° F of 275,1 K.
- Het presenteert een kookpunt in het bereik van 81,3 tot 82,1 ° C, een dichtheid van ongeveer 0,786 g/cm3 en een smeltpunt tussen -46 tot -44 ° C.
- Het is minder dicht dan water, maar mengbaar hiermee en met een verscheidenheid aan organische oplosmiddelen.
- Manifesteert een diëlektrische constante van 38,8 naast een dipoolmoment van ongeveer 3,92 d.
- Het is in staat om een breed scala aan stoffen van ionische oorsprong en niet -polaire aard op te lossen.
- Het wordt behoorlijk gebruikt als een mobiele fase in HPLC -analyse, die eigenschappen met hoge ontvlambaarheid presenteert.
Gebruik/toepassingen
Van het grote aantal toepassingen dat acetonitril heeft, kan het volgende worden geteld:
- Evenzo kan andere soorten nitrillen, dit kan een metabolisatieproces doorlopen in microsomen (vesiculaire elementen die deel uitmaken van de lever), vooral in dit orgaan, om cyanridinezuur te ontstaan.
- Het wordt op een zeer algemene manier gebruikt als een mobiele fase in het type analyse genaamd High Effective Inverse Phase Liquid Chromatography (RP-HPLC); dat wil zeggen, als de eluentstof met een hoge stabiliteit, grote eluent en verminderde viscositeit.
- In het geval van industriële magnitude -toepassingen wordt deze chemische verbinding gebruikt in ruwe olieraffinaderijen als een oplosmiddel in bepaalde processen, zoals de zuivering van de alkeen genaamd Butadieno.
- Het wordt ook gebruikt als ligand (chemische soorten die wordt gecombineerd met een atoom van een metaalelement, beschouwd als een centraal in het gegeven molecuul, om een coördinatieverbinding of complex te vormen) in een groot aantal nitrilverbindingen met metalen van de overgangsgroep.
- Evenzo wordt het gebruikt in de synthese van de organische type voor een groot aantal chemicaliën die zo voordelig zijn als a-naftaleenzuur, thiamine of acetamidinehydrochloride.
Risico's
De risico's die betrokken zijn bij blootstelling aan acetonitril zijn divers. Onder deze is een verminderde toxiciteit wanneer de blootstelling gedurende een verminderde periode en in lage hoeveelheden is, worden gemetaboliseerd voor de productie van cyanhydrinezuur.
Evenzo hebben er gevallen van mensen die zijn vergiftigd met deze chemische soorten, vergiftigd door cyanide aanwezig in het molecuul na in verschillende mate in contact te zijn geweest met acetonitril (bij het inademen, innemen of absorberen door de huid).
Kan u van dienst zijn: olie of benzine -ether: formule, structuur, gebruikOm deze reden worden de gevolgen van zijn toxiciteit vertraagd omdat het lichaam deze stof niet gemakkelijk in cyanide metaboliseert, omdat er twee tot twaalf uur nodig zijn om dit te laten gebeuren.
Acetonitril wordt echter gemakkelijk opgenomen in het gebied van de longen en het maagdarmkanaal. Vervolgens gebeurt de verdeling ervan in het hele organisme, gebeurt bij mensen en zelfs bij dieren en het bereiken van de nieren en de milt.
Aan de andere kant, naast de risico's van ontvlambaarheid die het presenteert, is acetonitril een voorloper van giftige stoffen zoals cyanhydric of formaldehydezuur. Zelfs het gebruik ervan in producten die behoren tot het cosmetische gebied in de So -Called European Economic Area in 2000.

